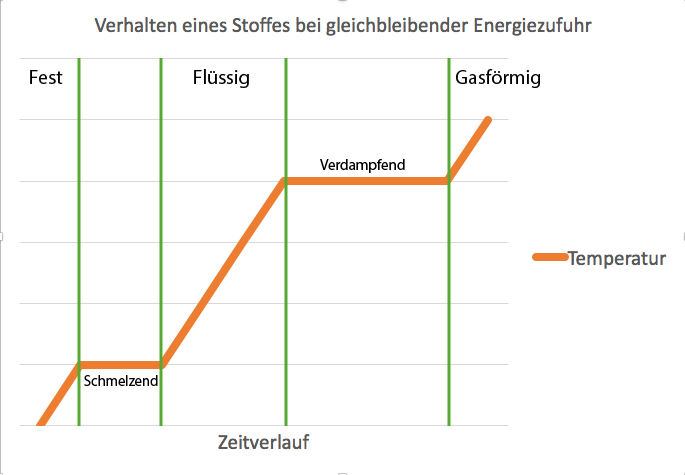
Die Veränderung eines Aggregatzustandes nennt man auch einen Phasenübergang. Während eines Phasenübergangs, bei dem ein Stoff seine Erscheinungsform ändert, behält dieser für kurze Zeit eine Übergangsform, in der die Temperatur konstant bleibt. Wenn ein Stoff zum Beispiel schmilzt behält dieser einen Zwischenzustand, welcher zwischen fest und flüssig liegt.
Dieses Verhalten tritt aufgrund der der Schmelzenthalpie auf. Die Schmelzenthalpie ist die benötigte Energie, um die zwischenatomaren Bindungskräfte eines Stoffes, der sich an seiner Schmelztemperatur befindet, zu lösen. Nach der Bereitstellung der benötigten Energie wird der Stoff dann flüssig. Diese benötigte Energie ist stoff- und druckabhängig.
Der entgegengesetzte Prozess der Schmelzenthalpie heißt Erstarrungsenthalpie. Während des Überganges von flüssig zu fest wird dabei Wärme freigesetzt. Dieser Effekt wird beispielsweise in der Landwirtschaft in einem kalten Frühling zur Erwärmung der Blüten eines Aprikosenbaumes verwendet.
Es gibt auch andere Arten der Enthalpie. Beispiele sind Verdampfungsenthalpie, Kondensationsenthalpie und Sublimationsenthalpie (Schmelzenthalpie + Verdampfungsenthalpie)